ちょうど1年経ったので:ノーベル化学賞2009解説—その1—
明日,2010年10月6日はノーベル化学賞の発表日だ.
ちょうど1年前,自分の専攻分野からノーベル化学賞が発表され,勢いにまかせて別ブログに解説記事を書いてみた.
徹夜明けの僕が語るよ「日本で二番目に早いノーベル化学賞2009解説」
本ブログの方が記事を掲載するのに適切なため,ちょうど1周年記念ということもあり,ノーベル化学賞2009解説記事を再編集して掲載する.
ちなみに僕は半人前の構造生物学者だが,リボソームの研究者ではないので要注意.
はじめに
2009年度ノーベル化学賞は
受賞理由
"for studies of the structure and function of the ribosome"
- リボソームの構造と機能に関する研究に対して
細胞内タンパク質合成装置であるリボソームの微細な立体構造の決定し,どうやってタンパク質が作られるか,その詳細を明らかにした研究が対象となった.
この研究を主導した3人の構造生物学者——結晶化を先駆的に進めたYonath*1,50Sを構造決定した Steitz*2,70Sを決定したRamakrishnan*3——が化学賞を受賞した.Steitzによる50S,Yonathによる30Sの構造決定はともに 2000年,Ramakrishnanによる全体構造の決定は2006年であり,受賞までに10年もかかっていない.もうリボソームにノーベル賞が出たか…,という印象だ.
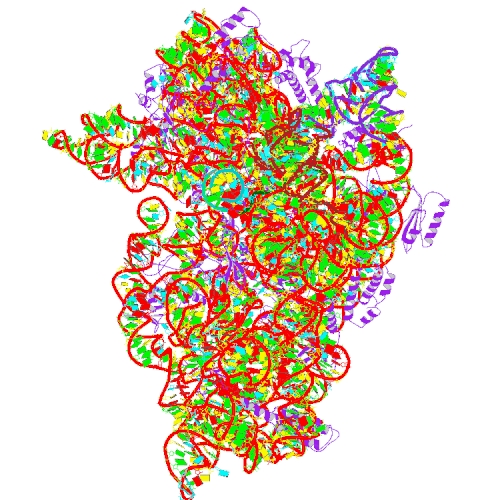
図1. 50Sリボソームの構造(PDBID: 2J00).
彼らの研究は
- 遺伝情報からタンパク質が作られるという,生物にとって基本中の基本と言える生化学反応の詳細なメカニズムを解明した
- 巨大な生体高分子の立体構造解析研究(構造生物学)としてのインパクトが多大であった
- 細菌感染症に対する新規抗生物質の開発という応用的意義が大きい
という3つの点が高く評価された.
ここでは,受賞した3人と惜しくも受賞を逃した1人の研究について紹介することで,構造生物学研究で最もエポックメイキングな研究でもある「リボソームの構造解析」について解説する.
前提知識
遺伝情報の流れ
DNAに刻まれた遺伝情報はDNA→RNA→タンパク質へと変換され,機能する.生命の設計図=DNAに書かれているのは,実は細胞の中で働くタンパク質の作り方.まずDNAの情報は,mRNAというコピーに「転写」される.mRNAはA, U, G, Cの4文字で書かれている.さらにmRNAからタンパク質へと遺伝情報は「翻訳」される.この翻訳を担うのがリボソーム.DNA,RNA,タンパク質は全て,カセットテープのように情報が一列に並んでいる(一次元的な情報媒体).
タンパク質
生命現象のメインプレイヤー.例えば,赤血球に含まれるヘモグロビンやパイナップルに含まれ肉をやわらかくする酵素パパインは,どちらもタンパク質.細胞の骨組みも,細胞内で起こる生化学反応も,ありとあらゆる生命現象はタンパク質の働きによって担われている.
タンパク質は,20種類のアミノ酸(例外あり)が順番に,1本の紐のように数珠つなぎになってできている.この紐(ポリペプチドと呼ばれる)が適切な形に折り畳まることで,タンパク質として機能を発揮する.アミノ酸の並び方によって,タンパク質の構造と機能は決まる.ヒトにはざっと10万種類くらいのタンパク質が存在する.
リボソーム
細胞内にあるタンパク質合成装置のこと.mRNAというテープの情報を読み取り,書かれている順番通りにアミノ酸をつなげることでタンパク質を作り出す.このステップは翻訳と呼ばれる.
リボソーム自身も,RNAとタンパク質という2種類の生体高分子からできた核酸-タンパク質複合体.直径は約200 nm,分子量260万.細胞内に存在する複合体としてはかなり巨大で,普通のタンパク質の100倍(分子量比)くらい.リボソームは細菌タイプと真核生物タイプの2種類がある.今回の研究は全て細菌タイプのリボソームについて行われた.細菌リボソームは大きく分けると,50Sリボソームと30Sリボソームという2つのブロックが組み合わさっている.リボソーム全体のことは70Sリボソームと呼ばれる*4.
リボソームの構造解析
ここまでは予備知識と言うことで,ここからは今回のノーベル賞受賞となった「リボソームの構造解析」について解説しよう.
カタチを見る生物学
図2. X線結晶構造解析の流れ.
今回受賞した3氏は,「X線結晶構造解析」と呼ばれる手法を用いて,リボソームの「詳細な立体構造」を決定する研究を行った.リボソームは
- mRNAに結合する
- アミノアシルtRNAを取り込む
- mRNAの情報を読み取って対応するアミノ酸をつなげていく
という機能を持っている.アミノアシルtRNAは,tRNAというアダプター分子にアミノ酸が結合したものであり.タンパク質合成の材料として使われる.
遺伝情報が翻訳されてタンパク質が作られることは,全ての生物にとって最も基本的な生命現象である.そのためリボソームの機能については,これまでに数々の研究が進められてきた.しかしながら,リボソームがどのようにmRNAやアミノアシルtRNAと結合し,どうやってmRNAの情報を読み取り,迅速かつ正確にアミノ酸をつなげていくのか,このメカニズムを明らかにするには,リボソームの構造や各ステップでの変化を「原子レベルで」詳細に観察する必要があった.例えて言うなら,馬がどうやって地面を蹴って走るかを知るには,高速連写した写真を撮る必要がある,というような話だ.
X線結晶構造解析とは?
原子レベルで立体構造を見るための方法としては,X線結晶構造解析,電子顕微鏡,NMRという3つの方法がある.今回の3氏が用いた方法はX線結晶構造解析である.
図3. 50Sリボソームの結晶.大きさは1 mm以下.
X線結晶構造解析とは生体高分子(タンパク質,DNA,RNAなど)の立体構造を決定するための手法の1つ.細胞内で働く生体高分子は非常に小さく,ヒトの身長を地球の直径にまで拡大した時,標準的なタンパク質は野球ボール〜バスケットボールくらいの大きさである.このように小さいものを,原子1つ1つを見分けられるレベルで形を決めるためには,顕微鏡ではなく特殊な方法が用いられる.
まず生体高分子を大量に精製し,特殊な条件で結晶化させる.この結晶にX線を当てて回折データを集め,コンピュータで色々頑張ることで立体構造を決めることができる.この方法を使うと,タンパク質を形作る炭素原子や酸素原子などが,どの位置にどう並んでいるかを明確に決めることができる.この「タンパク質のX線結晶構造解析法の開発」に対して,1962年にノーベル化学賞が与えられている.
ノーベル化学賞,4人の候補者たち
リボソームの詳細な立体構造を知るためには,まずリボソームを結晶化する必要がある.受賞者の1人Ada Yonathは,X線結晶構造学者としてずっとリボソームの結晶化を目指していた.「結晶化」という実験は試行錯誤だらけの世界.どうすればうまくいくかは分からず,ひたすら実験を繰り返して,運良く結晶化する条件を探し出さなければならない.またリボソームは巨大な生体高分子であるため,通常のタンパク質以上に結晶化が困難だった.しかし,Yonathたちは粘り強く研究を進めた結果,30Sと50Sの両方のリボソーム結晶化を世界で初めて成功した.これが90年代後半のこと.
しかし,構造を決定するためには,結晶化は最初のステップにすぎない.次に,結晶にX線を当てて「回折データ」を収集し,コンピュータで解析する必要がある.Yonathグループはリボソームの結晶化を世界に先駆けて成功させたが,構造を決定する部分では後れを取ってしまった.
ここで一歩リードしたのが,もう一人の受賞者Tom Steitzである.彼も結晶構造学者であり,リボソームの構造決定のために研究を行っていた.そして,Yonathが突き止めた結晶化条件を参考に自分達もリボソームの結晶を作り,回折データを収集・解析して,ついに50Sリボソームの結晶構造を決定に成功した*5.この発表が2000年8月11日.直後の9月1日,Yonathらも30Sリボソームの構造を発表する*6.この2つが世界初の「リボソームの詳細な立体構造」の報告となった.
さらにもう1人の受賞者Venki Ramakrishnanも,30Sリボソームと抗生物質との複合体構造を発表*7.これが9月21日.わずか1ヶ月あまりの発表ラッシュは,リボソーム立体構造の決定がどれだけ激しい競争であったかを物語っている.
しかし,これらの仕事の裏には,惜しくも受賞を逃したHarry Nollerの存在があった.そして,この時点ではまだリボソームの部分構造しか解明されていない.全体=70Sの構造が決定されるのは,ここからさらに6年の月日を待つこととなる.